檢測試劑組國家隊 進軍國際
試劑、快篩需求強勁,政府推專案法規放行,高端、普生、瑞基等估6月底前量產

新冠肺炎疫情風暴持續燃燒,全球確診人數破百萬人後仍一路攀高,檢測試劑、快篩需求強勁,為了加速國內相關檢測試劑廠商也能進軍國際,政府3月26日已祭出相關專案法規,加速審查流程,高端、普生、瑞基、奎克等廠商有機會搶頭香。而積極布局美國市場的瑞磁,則可望挾著4月底在美上市氣勢,回攻台灣和前進歐、亞市場。
生醫業界表示,由於國衛院單株抗體已率先完成活體病毒篩檢,4月8日將進行招商說明會,而中研院快篩試劑也將啟動技轉,加上專案法規放行,預估6月底前台灣檢測國家隊就可開始量產,全面在國內進行篩檢,並進軍國際。
目前由工研院研發的「手持核酸分子快篩系統」可望於4月底完成開發,而高端、瑞基的手持式PCR也有商業化實力。普生則是已接獲中東、東南亞地區訂單,奎克也有美國廠商尋求合作。而瑞磁則預計4月中向美國FDA申請緊急使用授權(EUA),初估4月底前應可上市,首批產能可篩檢10萬人。
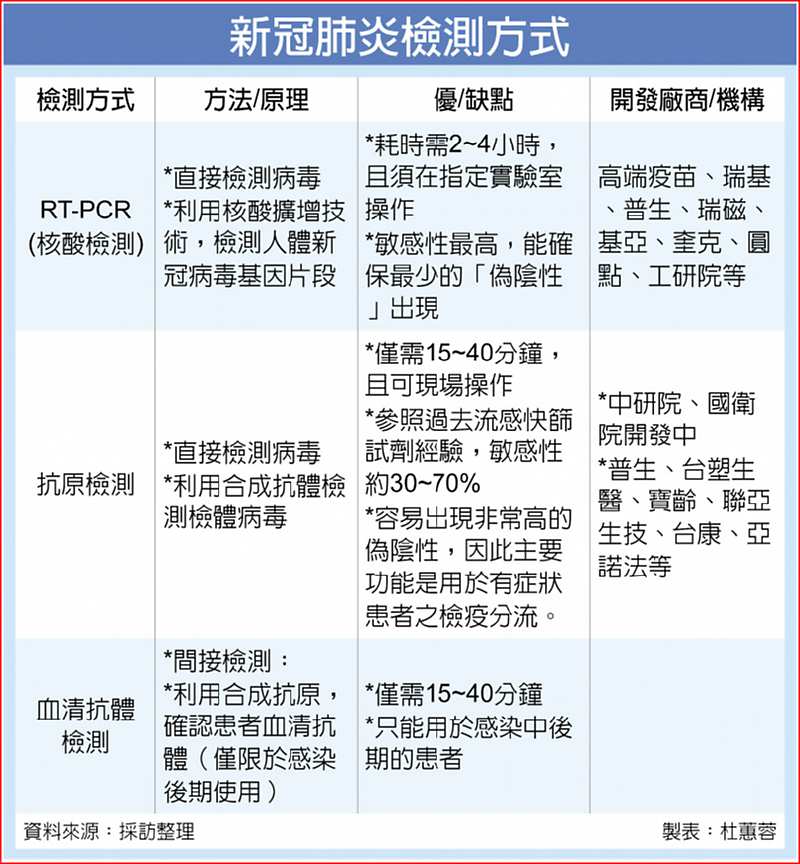
火力全開的檢測國家隊,目前是採三路並進方式布局,準確度最高的RT-PCR(目前全球的檢測方式),耗時雖需2~4小時,但敏感性最高,能確保最少的「偽陰性」出現,目前已有高端、瑞磁、普生、基亞、瑞基等廠商投入開發。
另外,速度最快的抗原檢測,則由中研院領軍,該快篩僅需15~40分鐘,但參照過去流感快篩試劑經驗,敏感性約30~70%,但因有助於檢疫分流,目前也有普生、台塑生醫、寶齡等廠積極布建產能。
至於血清抗體檢測,則有國衛院、生技中心等機構開發,該快篩試劑僅需15~40分鐘,但只能用於感染中後期的患者。
台灣生物產業發展協會理事長李鍾熙表示,因應疫情有兩個不同的廣度和面向,一是必須立即做好本土防疫,另一則是加速發展防疫產業,包括檢驗、快篩、藥物 、和疫苗等,以因應長期本土防疫需求,一方面也可進入國際市場, 協助全球防疫。
有鑑於新冠病毒正在全球肆虐,歐美地區疫情方興未艾,南半球國家也是岌岌可危,3月26日食藥署公告發布「新型冠狀病毒核酸檢測專案製造參考文件」及「新型冠狀病毒快篩試劑專案製造參考文件」,將有助於檢測國家隊成軍,並進軍海外市場,為產業帶來新的契機。